急性髓系白血病(Acute myeloid leukemia,AML)是最为常见的成人恶性血液肿瘤。其临床治疗仍然面临巨大挑战,目前多采用联合化疗方式,预后较差,5年总体生存率小于30%。因此,迫切需要深入探索急性髓系白血病发病机制、寻找新的治疗靶点和探索新的治疗策略。
2022年12月26日,武汉大学医学研究院/免疫与代谢前沿科学中心/口腔医学院/泰康生命医学中心张好建团队在Cell Stem Cell(《细胞-干细胞》)杂志在线发表了题为“Decoding m6A RNA methylome identifies PRMT6-regulated lipid transport promoting AML stem cell maintenance”的研究论文。该研究解码了急性髓系白血病发生过程中RNA m6A修饰动态变化,发现了关键分子PRMT6并阐明其调控疾病发生发展和白血病干细胞功能的重要作用与机制,为临床治疗提供潜在治疗策略。
在本研究中,研究人员解析了白血病起始细胞RNAm6A修饰组学,并与正常造血干祖细胞群体的m6A修饰组进行比较分析,全面解码急性髓系白血病发生过程中m6A修饰动态变化规律。研究人员发现m6A修饰阅读蛋白IGF2BP2在病人样品中高表达,并与患者不良预后息息相关;IGF2BP2缺失促进细胞凋亡,损伤白血病干细胞功能并抑制急性髓系白血病发生发展。有意思的是,研究人员发现了蛋白精氨酸甲基转移酶PRMT6是调控白血病干细胞干性的关键分子,并证实PRMT6 mRNA稳定性受到IGF2BP2调控,是IGF2BP2下游功能靶点。研究人员证实PRMT6维持白血病干细胞功能,发现PRMT6抑制剂EPZ020411能有效抑制白血病干细胞功能。同时,本研究进一步发现了PRMT6负调控脂质转运分子MFSD2A表达,从而影响脂肪酸比如二十二碳六烯酸DHA的转运,维持白血病干细胞功能。
综上,该研究将有助于我们深入理解急性髓系白血病发病机制,为其临床治疗提供重要理论依据和靶向新策略。据悉,该研究是张好建团队继2020年5月、2021年10月在Cell Stem Cell在线发表的两项工作的延伸。
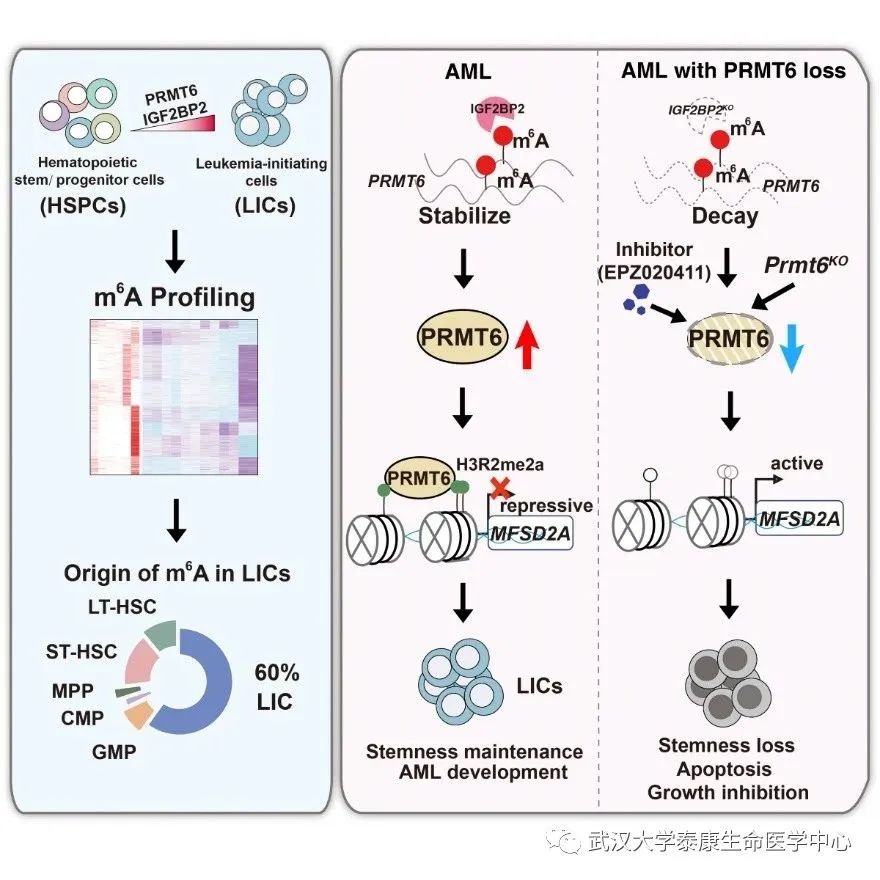
工作模式图:PRMT6催化H3R2me2a修饰抑制MFSD2A表达,维持白血病干细胞功能并促进急性髓系白血病发生发展
武汉大学医学研究院/免疫与代谢前沿科学中心博士生程颖、高竹英和张田田为文章的共同第一作者,张好建教授为文章通讯作者。武汉大学中南医院周芙玲教授、华中科技大学同济医学院附属协和医院黎玮明教授为本研究提供重要支持。该工作受到科技部重点研发计划干细胞专项、国家自然科学基金重点项目和青年项目、湖北省自然科学基金创新群体、武汉大学医学腾飞计划、中央高校自主科研项目等资助。
张好建课题组主要从事血液系统发育的分子机制和血液疾病的致病机理研究。目前研究方向包括血液系统细胞命运转化的调控机制、急性髓系白血病发病机制与靶向策略等。近三年来已在Cell Stem Cell(2022;2021;2020)、Blood(2021)、Cell Reports (2022)等发表多篇文章。
全文链接:https://doi.org/10.1016/j.stem.2022.12.003